电池-类型和工作
电池是用于大规模工业应用的手持设备最常见的电源。电池可以定义为;它是一个或多个电化学电池的组合,能够将储存的化学能转换成电能。

电池的工作:
电池是一种装置,由各种电压电池组成。每个Voltaic电池由导电电解质保持阴离子和猫离子串联连接的两个半电池组成。一个半电池包括电解质和阴离子移动的电极,即阳极或负电极;另一半电池包括电解质和猫离子移动的电极,即阴极或正极。
在为电池供电的氧化还原反应中,阴极处的阳离子发生还原,而氧化发生在阳极处的阴离子。电极不彼此接触,而是通过电解质电连接。大多数半细胞具有不同的电解质。考虑到每个半电池的所有内容都封闭在容器中,并且将隔膜与离子多孔,但不是电解质的大部分防止混合。
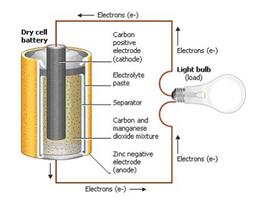
每半个电池都有一个电动势(Emf),由其驱动电流从电池内部到外部的能力决定。单元格的净电动势是其半单元格电动势之差。这样,如果电极有电动势,换句话说,净电动势是半反应的还原电势之间的差值。
如何维护电池?
为了保持电池处于良好的状态,电池平衡是必要的。由于老化,所有的细胞都不一样充电,有的细胞接受充电非常快,有的细胞逐渐充电。均衡可以通过稍微过度充电来实现,让较弱的电池也完全充电。完全充电的电池端电压为12v,汽车电池端电压为13.8V,管状电池端电压为12.8 v。汽车蓄电池应牢固地固定在车内,避免摇晃。如果可能,逆变器电池应放置在木板上。
2种电池类型
1)主要电池:
由于名称表示,这些电池用于单一使用。一旦使用这些电池,由于设备不易可逆,并且有源材料可能不会返回原始形式,因此不能再充电。电池制造商建议抵御原代细胞的充值。
一些一次性电池的例子是普通的AA、AAA电池,我们用在挂钟、电视遥控器等。这种电池的另一个名字是一次性电池。

2)二次电池:
二次电池也称为可充电电池。这些电池可以同时使用和充电。它们通常与处于放电状态的活性材料组装在一起。可充电电池是通过施加电流来充电的,电流会逆转放电过程中发生的化学反应。充电器是提供所需电流的装置。
例如,移动电话、MP3播放器等使用的充电电池。助听器和手表等设备使用微型电池,而在电话交换机或计算机数据中心等地方则使用较大的电池。

二次(充电)电池的种类:
SMF,铅酸,Li和Nicd
SMF电池:
SMF是A.密封免维护电池,专为UPS应用提供可靠、一致和低维护功率。在农村和电力不足的地区,这些电池可以满足深循环应用和最低维护要求。这些电池的电压为12V。
在当今信息化的世界,人们不能忽视对电池系统的要求,该系统旨在恢复关键的合格数据和信息,并运行基本仪器所需的时间。电池需要即时提供电力。不可靠和劣质电池可能导致数据丢失和设备关闭,给公司造成相当大的经济损失。随后,UPS部分要求使用可靠和可靠的电池系统。

锂电池(李):
我们都在便携式设备中使用它,如手机、笔记本电脑或电动工具。锂电池是近十年来便携式电源领域最伟大的成就之一;随着锂电池的使用,我们已经能够从黑白手机转变为彩色手机,并提供GPS、电子邮件提醒等附加功能。这些是具有更高容量的高能量密度的潜在器件。和相对较低的自放电电池。特殊电池还可以为电动工具等应用提供非常高的电流。

镍镉电池:
镍镉电池具有多次充电的优点,并且在放电期间具有相对恒定的电位,并且具有更大的电气和物质耐受能力。该电池使用用于阴极的氧化镍,用于阳极和氢氧化钾溶液的镉化合物作为其电解质。

当电池充电时,阴极化学成分发生变化,氢氧化镍转变为NIOOH。在阳极中,镉离子由氢氧化镉形成。当电池放电时,镉与NiOOH反应,形成背面的氢氧化镍和氢氧化镉。
Cd + 2H2O + 2NiOOH - > 2Ni(OH)2 + Cd(OH)2
铅酸蓄电池:
铅酸电池广泛用于汽车,逆变器,备用电源系统等。与管状和维护电池不同,铅酸电池需要适当的护理和维护,以延长其生命。铅酸电池由一系列板浸入硫酸溶液中的一系列板组成。板具有连接有活性材料的网格。将板分为正极板。阳性板将纯铅保持为活性材料,同时氧化铅附着在负极板上。
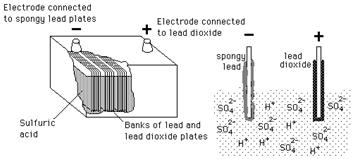
完全充电的电池在连接到负载时可以放电。在放电过程中,硫酸与正极和负极上的活性物质结合,形成硫酸铅。水是维护铅酸电池最重要的一个步骤。水的频率取决于使用、收费方式和操作温度。在此过程中,硫酸中的氢原子与氧反应生成水。
这导致从负极板接受的正板释放电子。这导致在电池中形成电势。铅酸电池中的电解质是具有比重的硫酸和水的混合物。与等同的水相比,比重是酸水混合物的重量。纯离子游离水的比重为1。
铅酸电池提供最佳的电力价值和每千瓦时的能量;拥有最长的生命周期和巨大的环境优势,因为它们的回收率极高。其他任何化学物质都无法与现有的收集、运输和回收铅酸电池的基础设施相媲美。
除了本文之外,锂离子电池讨论了其优点和缺点。
锂离子电池的工作

由于其持久的电源效率,锂电池现在流行了大多数电子便携式设备,如手机,笔记本电脑,数码相机等。这些是最流行的可充电电池,具有最佳能量密度,电荷损失可忽略不计,没有记忆效果。锂离子电池使用锂离子作为电荷载体,当充电时从负电极移动到正电极。在充电期间,来自充电器的外部电流施加超过电池中的电压。这迫使电流从正向到负极的反向传递,其中锂离子通过称为插入的过程嵌入多孔电极材料中。Li - 离子通过非含水电解质和隔膜隔膜。电极材料是插层锂化合物。
锂离子电池的负极由碳组成,正极是金属氧化物。负电极中最常用的材料是石墨,而正极中可以是钴氧化物,锂离子磷酸锂或锂锰氧化物。有机溶剂中的锂盐用作电解质。电解质通常是碳酸亚乙酯或含锂离子的碳酸亚乙酯的有机碳酸酯的混合物。电解质使用锂六氢氟磷酸锂,六氢氟代酸锂盐,每氯酸锂,锂六氢氟硼酸锂等,取决于所用的盐,电池的电压,容量和寿命变化。纯锂剧烈使水剧烈形成氢氧化锂和氢离子。所以使用的电解质是非水性有机溶剂。电极电荷在阳极和阴极之间的电化学作用取决于电流的方向。
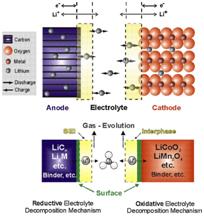
在锂离子电池中,两个电极都可以接受和释放锂离子。在插入过程中,锂离子进入电极。在称为脱嵌层的反向过程中,锂离子向后移动。在放电过程中,正锂离子将从负极中提取并插入正极。在充电过程中,锂离子发生反向运动。
锂离子电池的优势:
锂离子电池优于NICD电池和其他二次电池。一些优点是
- 轻量级与其他相似电池相比
- 可提供不同的形状,包括平面形状
- 在低电流下增加功率传输的高开路电压
- 缺乏记忆效果。
- 自放电率极低,每月5-10%。镍镉电池和镍氢电池的自放电率约为30%。
- 不含游离锂金属的环保电池
但与其他电池一样,锂离子电池在优点的同时也存在一些缺点。
锂离子电池的缺点:
- 电解液内的沉积物随着时间的推移会抑制电荷的流动。这增加了电池的内阻,电池的电流输出能力逐渐降低。
- 充电过高、温度过高可能导致容量损失
- 当温度过高时,锂离子电池可能会发生热流失和电池破裂。
- 深放电可能导致锂离子电池短路。因此,为了防止这种情况,一些制造商有内部关闭电路,当其电压高于3至4.2伏特的安全水平时,关闭电池。在这种情况下,当电池长时间不使用时,内部电路会消耗电能,并在电池关机电压以下耗尽电池。所以要给这种电池充电,普通的充电器是没有用的。





Thanx为信息伙伴。我真的需要这个信息,在这里我得到了这个。
谢谢
非常棒的关于电池的描述,任何人都会对电池有一个清晰的概念,阅读你的文章真的很有帮助,谢谢。
感谢分享这篇信息丰富的文章。解释清楚的锂离子电池。
阴极就是负极
这个博客提供了很多关于电池的信息,我在这里找到了最好的东西。